Optogenetik
Die Optogenetik-Gruppe entwickelt genetisch kodierte, licht-aktivierte Werkzeuge zur Untersuchung der Biophysik kardialer Prozesse – von Signalen einzelner Zellen bis hin zur mechano-elektrischen Aktivität des gesamten Herzens. Derzeit konzentrieren sich unsere Forschungsaktivitäten auf drei Hauptthemen:
(1) die Entwicklung und Anwendung neuartiger licht-gesteuerter Ionenkanäle zur Modulation der Herzmuskelzell-Aktivität,
(2) die Untersuchung der heterozellulären Kopplung zwischen Kardiomyozyten und interstitiellen Herzzellen, sowie
(3) die Erforschung der neuronalen Steuerung der Herzfunktion.
Neuartige lichtgesteuerte Ionenkanäle
Im letzten Jahrzehnt haben wir zur Entwicklung und funktionellen Testung neuer licht-gesteuerter Ionenkanäle beigetragen, insbesondere haben wir die neu entdeckten Gruppen von lichtgesteuerten Chlorid- und Kaliumkanälen erforscht. Mithilfe von Patch-Clamp-Messungen, Kontraktionsverfolgung und computergestützter Modellierung testen wir systematisch den Einfluss der biophysikalische Kanaleigenschaften auf die Kardiomyozytenaktivität. Aktuell untersuchen wir, wie die Ionenselektivität lichtgesteuerter Kanäle deren Potenzial zur Beendigung von Reentry-Arrhythmien im Herzen bestimmt. Dieses Projekt wird vom Medical Scientist Programme der DGK gefördert.
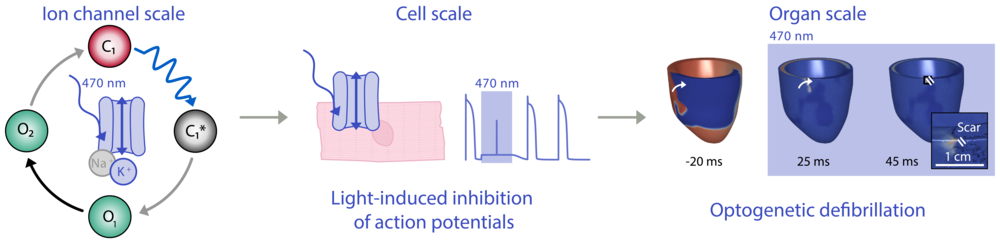
Charakterisierung lichtgesteuerter K⁺-Kanäle über verschiedene Skalen hinweg. Links: Vereinfachtes Fotozyklus-Modell. Mitte: Hemmung von Aktionspotenzialen in Kardiomyozyten. Rechts: Simulation der durch K⁺-Kanäle vermittelten Defibrillation einer Reentry-Arrhythmie im menschlichen Ventrikel.
Heterozelluläre Kopplung zwischen Kardiomyozyten und Interstitialzellen
Im nativen Myokard sind Kardiomyozyten von interstitiellen Nicht-Myozyten umgeben, die die elektromechanische Aktivität des Herzens prägen. Wir untersuchen die bidirektionale biophysikalische Kommunikation zwischen Muskel und Interstitium und deren Auswirkungen auf die Herzfunktion unter physiologischen und pathophysiologischen Bedingungen. Dazu nutzen wir Optical Mapping und optogenetische Manipulation, 3D-Bildgebung optisch geklärter Proben, und in silico-Modelle. Diese Aktivitäten sind in die neu gegründete Forschungsgruppe FOR6051 eingebettet.
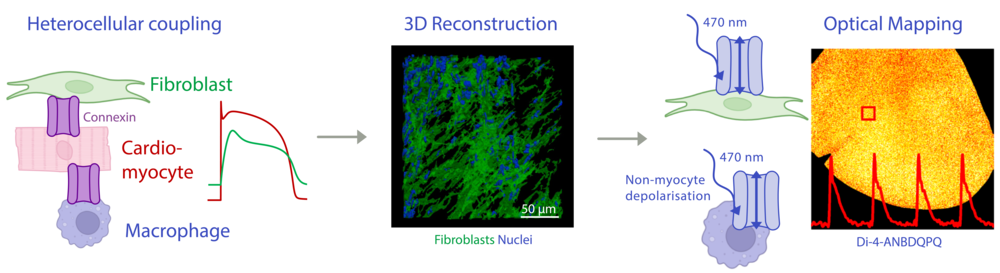
Effekte der heterozellulären elektrotonischen Kopplung zwischen Kardiomyozyten und interstitiellen Nicht-Myozyten. Links: Schematische Übersicht. Mitte: 3D-Rekonstruktion eines Fibroblastennetzwerks in ventrikulärem Narbengewebe. Rechts: Funktionelle Experimente kombinieren die optogenetische Stimulation von Nicht-Myozyten mit farbstoffbasierter optischer Kartierung des Membranpotenzials.
Neuronale Steuerung der Herzfunktion
Mithilfe eigens entwickelter optogenetischer Verfahren untersuchen wir, wie die Aktivität des autonomen Nervensystems die kardiale Elektrophysiologie und Kalziumdynamik beeinflusst und ob eine Dysregulation der neuronalen Balance die Entstehung von Herzrhythmusstörungen begünstigen kann. Wir schlagen eine Brücke von der Charakterisierung neurokardialer Verbindungen im Mikrometer-Maßstab zur Elektrophysiologie des gesamten Herzens und untersuchen zudem die nachgeschaltete Integration ausgewählter G-Protein-Signalwege in Kardiomyozyten und Nicht-Myozyten. Diese Projekte werden durch FOR5807 und einen ERC Synergy Grant gefördert.
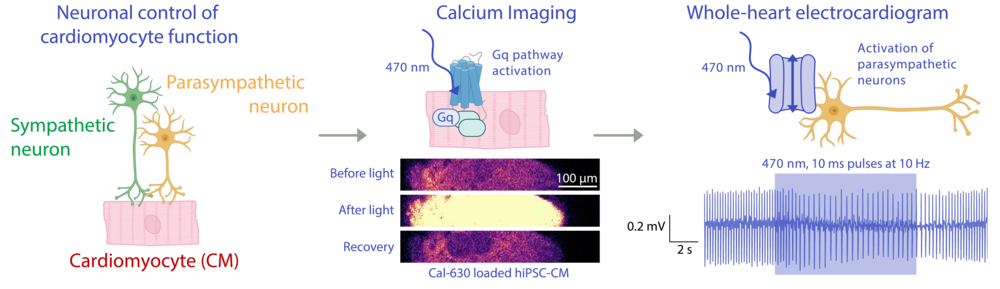
Optogenetische Untersuchung von Neuronen-Herzmuskelzell-Kommunikation. Links: Schematische Darstellung der beteiligten Zelltypen. Mitte: Optogenetische Aktivierung des Gq-Protein Signalweges, visualisiert durch Kalzium-Imaging. Rechts: Optogenetische Stimulation parasympathischer Neurone verringert die Herzfrequenz.
- Ohnemus S, Tillert L, De Zio R […] Leemisa AN […] Kohl P, Timmermann V, Schneider-Warme F, Vierock J. Experimentally informed, quantitative photocycle model of the light-gated potassium channel WiChR. Biophys J 2026/in press
- Spreen A, Sadanandan N, Schneider MW […] Leemisa AN, De Zio R […] Heer J […] Schneider-Warme F, Bernal Sierra YA, Seifert R. Optogenetic silencing by combining a rhodopsin cyclase with an engineered cGMP-gated potassium channel. Sci Adv 2025/11:eadx1195
- Stefanovska D, Sassu E, Tekman M […] Perez-Feliz S […] Schneider-Warme F […] Preissl S, Hortells L. Fibroblast growth factor signaling induces a chondrocyte-like state of peripheral nerve fibroblast during aging. Nat commun 2025/16:10020
- Chan A, Greiner J, Marschhäuser L, Brennan TA, Perez-Feliz S […] Klesen A […] Rog-Zielinska E, Kohl P, Schneider-Warme F, Grün D. Spatio-temporal dynamics of the cardio-immune niche during lesion repair. Nat Cardiovasc Res 2025/4:1550-1572
- Simon-Chica A, Klesen A, Emig […] Greiner J […] Rog-Zielinska EA, Ravens U, Kohl P, Schneider-Warme F, Peyronnet R. Piezo1 stretch-activated channel activity differs between murine bone marrow-derived and cardiac tissue-resident macrophages. J Physiol 2024/602:4437-4456
- Sassu E, Tumlinson G, Stefanovska G, Fernández MC, Iaconianni P, Madl J, Brennan TA, Koch M, Cameron BA […] Ravens U, Schneider-Warme F, Kohl P, Zgierski-Johnston CM, Hortells L. Age-related structural and functional changes of the intracardiac nervous system. J Mol Cell Cardiol 2024/187:1-14
- Vierock J, Peter E, Grimm C […] Casini M […] Peyronnet R, Schneider-Warme F […] Hegemann P. WiChR, a highly potassium-selective channelrhodopsin for low-light one- and two-photon inhibition of excitable cells. Sci Adv 2022/8:eadd7729
- Simon-Chica A, Fernández MC, Wülfers EM, Lother A, Hilgendorf I, Seemann G, Ravens U, Kohl P, Schneider-Warme F. Novel insights into the electrophysiology of murine cardiac macrophages: relevance of voltage-gated potassium channels. Cardiovasc Res 2022/118(3):798-813
- Kopton RA [...] Moss R, Zgierski-Johnston CM [...] Kohl P, Quinn TA, Schneider-Warme F. Cardiac Electrophysiological Effects of Light-Activated Chloride Channels. Front Physiol 2018/9:1806
- Bernal Sierra YA*, Rost BR*, Pofahl M* [...] Kopton RA [...] Kohl P, Baier H, Schneider-Warme F [...] Schmitz D. Potassium channel-based optogenetic silencing. Nat Commun 2018/9:4611 (*equal contribution)
Team

Dr. Franziska Schneider-Warme
Arbeitsgruppenleiterin

Jan Rebers
E-Mail: jan.rebers@uniklinik-freiburg.de

Roberta De Zio, PhD
Guest Scientist

Ana Simón Chica, PhD
Guest Scientist