Translationale Medizinische Forschung
Diese Sektion verbindet die Forschung des Instituts für Experimentelle Kardiovaskuläre Medizin mit der klinischen Praxis an der Uniklinik Freiburg.
Prävention von Ischämie-Reperfusionsarrhythmien
Ein Herzinfarkt entsteht typischerweise durch den Verschluss einer Koronararterie, was zur Ausbildung eines ischämischen Areals führt. Die Beseitigung dieses Verschlusses ist notwendig, um die Gewebegesundheit wiederherzustellen, kann jedoch paradoxerweise zusätzliche Schädigungen verursachen, einschließlich von Herzrhythmusstörungen.
Kürzlich haben wir einen neuartigen Mechanismus dieser Ischämie-Reperfusionsarrhythmien identifiziert, der auf “PeriVaskulären ErregungsTunneln” basiert (Chleilat et al.). Dabei erlangt das Myokard in unmittelbarer Nähe des Hauptasts des verschlossenen Koronargefäßes zuerst wieder seine Erregbarkeit zurück, wodurch ein Art ”Leitungskorridor" durch das zuvor ischämische Gewebe entsteht.
Im Rahmen eines durch das BMFTR geförderten Projekts entwickeln wir gemeinsam mit der OSYPKA GmbH einen neuartigen Reperfusionskatheter, der in Pilotversuchen das Auftreten von Arrhythmien vollständig verhindert. Die laufenden Arbeiten in diesem Projekt umfassen die Optimierung des Katheterdesigns, seiner Anwendung und Handhabung sowie den Einsatz in isolierten Herzen und in vivo, mit dem langfristigen Ziel, Arrhythmien bei PatientInnen zu verhindern und die klinischen Ergebnisse nach Herzinfarkt zu verbessern.
Dieses Projekt wird von Callum Zgierski-Johnston geleitet.
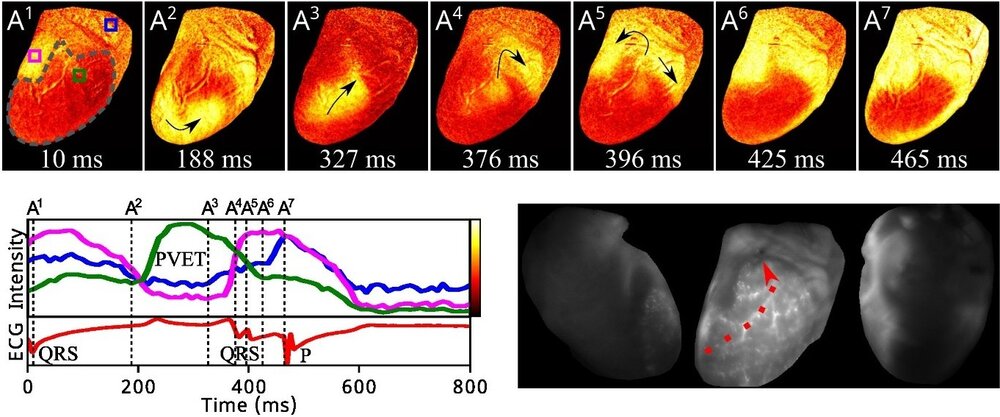
Abb. 1: Arrhythmie nach Reperfusion. A1–A7: Bildsequenzen, die die kardiale Erregungsausbreitung durch die zuvor ischämische Zone (graue gestrichelte Linien) zeigen, was zur Wiedererregung des gesamten Herzens führt. Unten links: Intensitäten aus den in A1 dargestellten Regionen von Interesse sowie das entsprechende Elektrokardiogramm, das die invertierte Erregungsabfolge demonstriert (QRS-Komplex gefolgt von P-Welle). Unten rechts: Aufnahme nach Perfusion mit fluoreszierenden Mikrosphären, die den Hauptast der perfundierten Koronararterie zeigt.
Verbesserung von Ablationsverfahren
Vorhofflimmern ist eine der häufigsten kardialen Arrhythmien. Zu den aktuellsten Therapieansätzen zählt die gepulste Feldablation (pulsed-field ablation), bei der kurze hochspannungsbasierte elektrische Impulse eingesetzt werden, um irreversible Poren in Herzmuskelzellen zu erzeugen. Dadurch wird die elektrische Erregungsleitung unterbrochen und die Arrhythmie beendet.
Im Rahmen eines durch das BMFTR geförderten Projekts arbeiten wir mit industriellen Partnern zusammen, die Generatoren und Kathetersysteme entwickeln, um die Mechanismen der Läsionsbildung sowie die Parameter, die die Läsionsmorphologie bestimmen, besser zu verstehen. Mithilfe translationaler Modelle und humanen Gewebes aus der CVBB-Biobank evaluieren wir die Effizienz der gepulsten Feldablation durch eine Kombination verschiedener Methoden, darunter optisches Mapping, Live/Dead-Zellfärbungen sowie histologische Verfahren.
Durch die Integration experimenteller Forschung mit Methoden der künstlichen Intelligenz, in Zusammenarbeit mit dem Karlsruher Institut für Technologie, verfolgen wir langfristig das Ziel, Ablationsprotokolle an spezifische Gewebeeigenschaften und letztlich an individuelle Patientinnen und Patienten anzupassen.
Erste Ergebnisse dieses Projekts wurden auf der Jahrestagung der Deutschen Gesellschaft für Kardiologie (DGK) ausgezeichnet.
Dieses Projekt wird von Rémi Peyronnet geleitet.
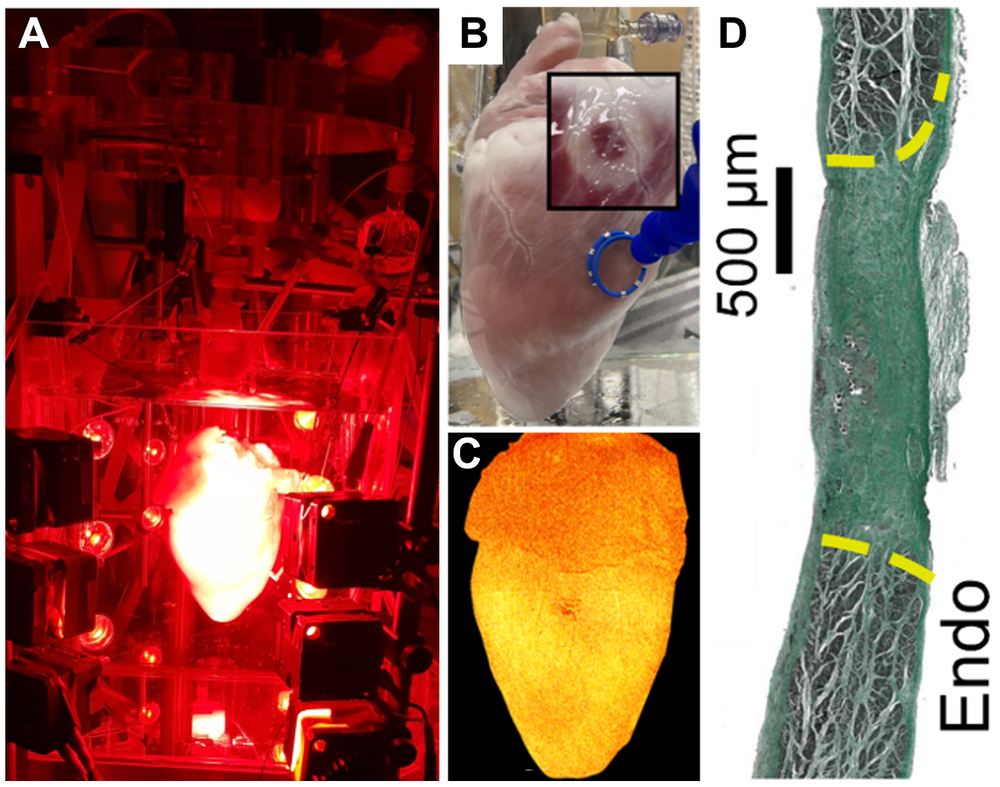
Fig. 2: Ablationen ex vivo und in vivo. A) Ablationen werden an einem Langendorff-perfundierten Herzen durchgeführt, wobei ihre Auswirkungen auf die elektrische Erregungsleitung mittels optischem Mapping überwacht werden.
B) Beispielhaft dargestellte Läsionen unter Verwendung eines Live-Cell-Markers (rotes Gewebe in den Insets zeigt metabolisch aktive Zellen, während weiße Areale die Läsion bzw. abgestorbene Zellen repräsentieren).
C) Aufnahme eines Herzens, das mit einem spannungssensitiven Farbstoff beladen ist, welcher seine elektrische Aktivität abbildet.
D) Beispiel einer Narbe nach in vivo durchgeführter Ablation und anschließender Regeneration, charakterisiert mittels hochdurchsatzfähiger Bildgebung sowie histologischer Verfahren.