4D Bildgebung / Kardiale NanoDynamiken
In der Sektion 4D Bildgebung verwenden wir experimentelle Ansätze, um die dynamische kardiale Ultrastruktur auf der Nano- bis Mikroskala zu untersuchen. Im Rahmen unserer Forschung versuchen wir zu verstehen, wie die verschiedenen Zellen des Herzens auf ihre Umgebung reagieren, beispielsweise auf mechanische Reize (wie Kontraktionen) oder auf Signale, die von benachbarten Zellen ausgehen.
Hauptforschungsgebiete sind:
Ultrastruktur und Funktion subzellulärer Domänen im schlagenden Herzen
Die äußerlich erscheinende Gleichförmigkeit der Kontraktionen der Herzmuskelzellen resultiert aus der Koordination zahlreicher, räumlich und zeitlich heterogener Prozesse, die spezialisierte subzelluläre Nanodomänen einbeziehen. Wir untersuchen die Herzschlag-zu-Herzschlag-basierte Autoregulation der Herzfunktion auf der Nanoskala und postulieren, dass der Herzschlag nicht lediglich das Ergebnis der Aktivität von Herzmuskelzellen ist, sondern einen intrinsischen Regulator darstellt, der die Struktur und Funktion von Nanodomänen kontinuierlich modifiziert, um das System auf den nächsten Herzschlag vorzubereiten.
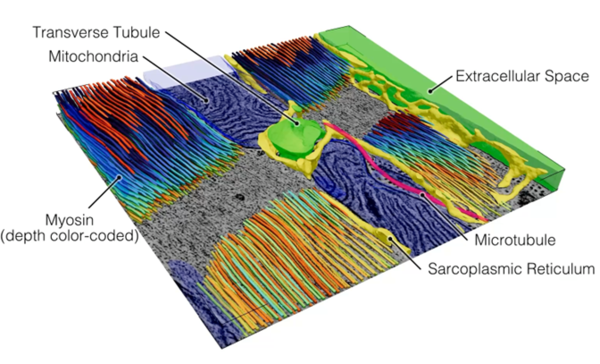
Hierzu setzen wir zeitaufgelöste dreidimensionale Elektronenmikroskopie, subzelluläre funktionelle Bildgebung, ultrastrukturelle Proteomik sowie KI-gestützte Datenanalyse ein, um die ultrastrukturelle Dynamik des Herzens auf der Skala von Nanometern und Millisekunden zu kartieren.
Segmentierung von Organellen von Herzmuskelzellen in einem 3D-Elektronentomographie-Volumen. Bild: Dr. J. Greiner.
Interaktion zwischen Herzmuskel- und Bindegewebszellen im Herzen
Wir untersuchen die nanoskaligen Interaktion zwischen Herzmuskelzellen (Kardiomyozyten) und Bindegewebszellen (Fibroblasten) im Kontext des fibrotischen Gewebeumbaus. Insbesondere analysieren wir die Rolle dynamischer fibroblastärer Membran-Nanotubuli im Prozess der extrazellulären Matrixablagerung an der Schnittstelle zu Kardiomyozyten sowie innerhalb kardialer Nanodomänen.
Hierzu verwenden wir zeitaufgelöste Licht- und Elektronenmikroskopie, Modelle humaner induzierter pluripotenter Stammzellen (hiPSC) sowie Proteomik, um Einblicke in nanoskalige Mechanismen des fibrotischen Gewebeumbaus zu gewinnen und Strategien zur gezielten Modulation der Fibroblasten-Kardiomyozyten Interaktionen zu entwickeln.
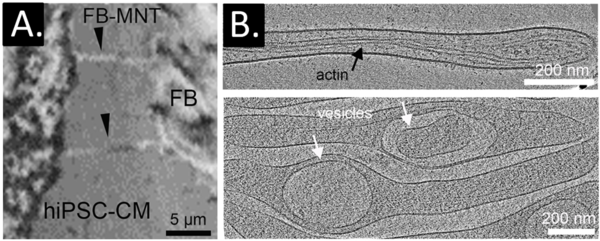
A: Kokultur aus primären humanen kardialen Fibroblasten (FB, rechts) und hiPSC-Kardiomyozyten (links); fibroblastäre Membran-Nanotubuli (FB-MNT) interagieren direkt mit den Membranen der hiPSC-Kardiomyozyten.
B: Fibroblastäre Membran-Nanotubuli können mittels 3D-Kryo-Elektronentomographie visualisiert werden. Innerhalb der fibroblastären Membran-Nanotubuli werden zahlreiche Strukturen nachgewiesen, darunter Aktin, Vesikel sowie Organellen wie Mitochondrien
Interaktion zwischen Herzmuskel- und Nervenzellen im Herzen
Das intrakardiale Nervensystem spielt eine zentrale Rolle bei der fein abgestimmten Regulation der Herzfunktion. Die Effizienz und Präzision der neuro-kardialen Kommunikation werden maßgeblich durch die ultrastrukturelle Geometrie der Schnittstelle zwischen Nervenzellen (Neuronen) und Herzmuskelzellen (Kardiomyozyten) bestimmt. Trotz ihrer funktionellen Bedeutung ist die nanoskalige Architektur und dynamische Organisation der neuro-kardialen Synapse bislang nur unzureichend verstanden.
Wir untersuchen die strukturelle Organisation und funktionellen Eigenschaften der neuro-kardialen Schnittstelle auf der Nanoskala unter Verwendung von hiPSC-Modellen sowie modernen hochauflösenden Bildgebungsverfahren.
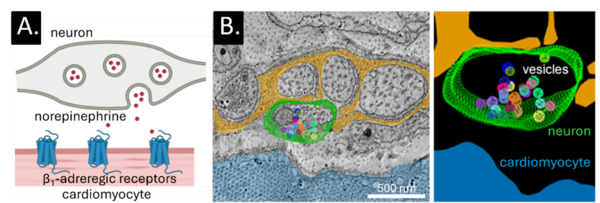
A: Schematische Darstellung der vermuteten Struktur der neuro-kardialen Schnittstelle, die einen sympathischen Nervenendknopf zeigt, welches eine enge synapsenähnliche Annäherung an einen Kardiomyozyten ausbildet. Dabei sind die Stellen für Vesikelfreisetzung direkt gegenüber den postsynaptischen Rezeptoren positioniert.
B: Dreidimensionale Elektronenmikroskopie und Rekonstruktion unmyelinisierter Nervenfasern im Sinusknoten der Maus.
- Mechanische Verformung der Ultrastruktur von Herzmuskelzellen - Struktur und Funktion
- Entwicklung neuartiger lebender fluoreszenter Ionenindikatoren
- Korrelative Licht- und Elektronenmikroskopie
- Nanoskalige Mechanismen des fibrotischen Remodellings
- Organotypische Schnittkulturmodelle
- Neuron-Kardiomyozyten-Crosstalk
- Rog-Zielinska EA, Grune J, Kessler T, Lother A, Kohl P. Interstitial cells and arrhythmia. Am J Physiol Cell Physiol 2026/330:C943-C953
- Orós-Rodrigo S, Fu J, Greiner J, Madl J […] Zgierski-Johnston CM [...] Kohl P, Rog-Zielinska EA. Cardiomyocyte mechanical activity counteracts intraluminal calcium depletion in the transverse-axial tubular system during fast electrical stimulation. bioRxiv 2026
- Greiner J, Sonak F, Jones WD, Madl J […] Kohl P, Rog-Zielinska EA. Architecture of the cardiac transverse-axial tubular system across different mammalian species. bioRxiv 2026
- Greiner J, Frangiamore F, Sonak F, Madl J, Seidel T, Kohl P, Rog-Zielinska EA. A deep learning-enabled toolkit for the 3D segmentation of ventricular cardiomyocytes. J Physiol 2025/in press
- Pronto JRD, Mason FE, Rog-Zielinska EA […] Voigt N. Impaired atrial mitochondrial calcium handling in patients with atrial fibrillation. Circ Res 2025/137:1333-1352
- Fu J, Cameron BA […] Schiatti T […] Madl J […] Ravens U, Kohl P, Rog-Zielinska EA, Antoons G, Peyronnet R. Stretch-induced increase in Ca2+-spark rate in rabbit atrial cardiomyocytes requires transient receptor potential ankyrin 1 and intact microtubule network. J Am Heart Assoc 2025/4:e040495
- Greiner J […] Oros-Rodrigo S, Cameron BA, Madl J, Kaltenbacher W, Kok T, Zgierski-Johnston CM, Peyronnet R, Kohl P, Sacconi L, Rog-Zielinska EA. Different effects of cardiomyocyte contractile activity on transverse and axial tubular system luminal content dynamics. J Mol Cell Cardiol 2024/197:125-135
- Paulke NJ […] Lenz C, Rog-Zielinska EA, Lehnart SE, Brandenburg S. Dysferlin enables tubular membrane proliferation in cardiac hypertrophy. Circ Res 2024/135:554-574
- Kohl P, Greiner, J, Rog-Zielinska EA. Electron microscopy of cardiac 3D nanodynamics: form, function, future. Nat Rev Cardiol 2022/19:607-619
- Jünger F [...] Daller CC, Rog-Zielinska EA [...]. 100 Hz ROCS microscopy correlated with fluorescence reveals cellular dynamics on different spatiotemporal scales. Nat Commun 2022/13:1758
- Rog-Zielinska EA, Moss R, Kaltenbacher W, Greiner J, Verkade P, Seemann G, Kohl P, Cannell MB. Nano-scale morphology of cardiomyocyte t-tubule/sarcoplasmic reticulum junctions revealed by ultra-rapid high-pressure freezing and electron tomography. J Mol Cell Cardiol 2021/153:86-92
- Rog-Zielinska EA [...] Peyronnet R, Zgierski-Johnston, Greiner J, Madl J [...] Kohl P. Beat-by-beat cardiomyocyte T-tubule deformation drives tubular content exchange. Circ Res 2021/128:203-215
- MacDonald EA, Madl J, Greiner J […] Rog-Zielinska EA*, Quinn TA*. Sinoatrial node structure, mechanics, electrophysiology and the chronotropic response to stretch in rabbit and mouse. Front Physiol 2020/11:908 (*joint authorship)
- Kong CHT*, Rog-Zielinska EA*, Kohl P, Orchard CH, Cannell MB. Solute movement in the t-tubule system of rabbit and mouse cardiomyocytes. PNAS USA 2018/115:E7073-E7080 (*joint authorship)
- Rog-Zielinska EA, O'Toole ET, Hoenger A, Kohl P. Mitochondrial Deformation During the Cardiac Mechanical Cycle. Anat Rec 2018/302:146-152
- Scardigli M [...] Rog-Zielinska EA, Kohl P [...] Sacconi L. Quantitative assessment of passive electrical properties of the cardiac T-tubular system by FRAP microscopy. PNAS USA 2017/114:5737-5742
- Brandenburg S [...] Rog-Zielinska EA [...] Kohl P [...] Lehnart SE. Axial tubule junctions control rapid calcium signaling in atria. J Clin Invest 2016/126:3999-4015
- Quinn TA*, Camelliti P*, Rog-Zielinska EA* [....] Kohl P. Electrotonic coupling of excitable and non-excitable cells in the heart revealed by optogenetics. PNAS USA 2016/113:14852-14857 (*joint authorship)
- Rog-Zielinska EA, Johnston CM [...] Kohl P. Electron tomography of rabbit cardiomyocyte three-dimensional ultrastructure. Prog Biophys Mol Biol 2016/121:77-84
- Rog-Zielinska EA, Norris RA, Kohl P, Markwald R. The Living Scar - Cardiac Fibroblasts and the Injured Heart. Trends Mol Med 2016/22:99-114
Team

Eva Rog-Zielinska, PhD
Arbeitsgruppenleiterin

Dr. Josef Madl
Senior Scientist
E-Mail: josef.madl@uniklinik-freiburg.de

Hannah Kappler

Sofía Orós Rodrigo

Patricia Aparecida Morais Costa

Wenzel Kaltenbacher

Wesley Dean Jones

Nina Steinhagen

Eric Suaudeau

Jana Meyer
E-Mail: jana.meyer@uniklinik-freiburg.de

Jaide Cashin